Vụ 20.000 viên thuốc ung thư bị tiêu hủy: Bộ Y tế khẳng định đúng quy trình cấp phép
Sức khỏe - Ngày đăng : 08:37, 09/05/2017
Liên quan đến thông tin về gần 20.000 viên thuốc Tasigna đặc trị ung thư buộc phải tiêu hủy, chiều 8/5, Cục Quản lý Dược (Bộ Y tế) cho biết, ngay khi nhận được thông tin về 20.000 viên thuốc Tasigna đặc trị ung thư buộc phải tiêu hủy, cơ quan này đã yêu cầu Sở Y tế thành phố Hồ Chí Minh báo cáo về vụ việc trước ngày 7/5. Tuy nhiên đến thời điểm hiện tại, Cục Quản lý Dược vẫn chưa nhận được báo cáo về vụ việc này.
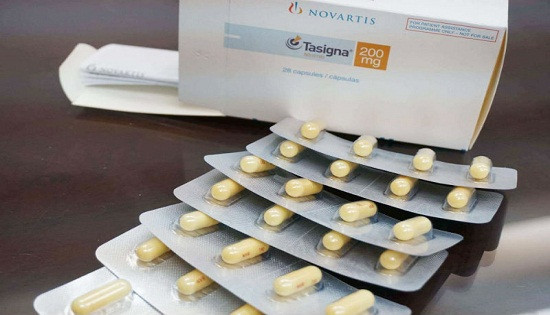
Thuốc Tasigna 200mg đặc trị bệnh bạch cầu mạn dòng tủy.
Cục quản lý Dược cũng khẳng định việc cấp phép nhập khẩu thuốc Tasigma đã được thực hiện đúng theo quy định tại khoản 2 Điều 16 Thông tư 47/2010/TT-BYT hướng dẫn hoạt động xuất khẩu, nhập khẩu thuốc và bao bì tiếp xúc trực tiếp với thuốc và đáp ứng quy định về thời gian không quá 15 ngày làm việc.
Trước đó, ông Phù Chí Dũng- Giám đốc Bệnh viện Truyền máu & Huyết học TPHCM tổ chức họp đồng thời lý giải việc tồn kho gần 20.000 viên thuốc đặc trị ung thư Tasigna.
Theo ông, qui trình nhập được thuốc về quá khó khăn và phức tạp, kéo dài đúng 1 năm. Đến cuối tháng 7/2013, bệnh viện đang có 200 bệnh nhân điều trị do mắc căn bệnh bạch cầu tuỷ cần thuốc điều trị. Tuy nhiên, do phụ thuộc vào thủ tục xin tiếp nhận thuốc của các cơ quan chức năng quá lâu nên nhiều bệnh nhân trong số này không tham gia điều trị.

BS Phù Chí Dũng - Giám đốc Bệnh viện Truyền máu huyết học TP.HCM giải thích về nội dung kết quả thanh tra
Trước đó như Báo Công lý đã đưa tin, liên quan đến thông tin gần 20.000 viên thuốc Tasigna đặc trị ung thư buộc phải tiêu hủy; Tổng cục Hải quan cũng khẳng định, việc lô hàng thuốc còn lại hạn dùng quá ít khi hoàn thành thủ tục nhập khẩu không phải do hải quan kéo dài thời gian làm thủ tục. Vì lý do nhân đạo, hải quan vẫn nhanh chóng thông quan lô hàng 1 ngày kể từ ngày đăng ký tờ khai hải quan. Phía hải quan khẳng định cơ quan hải quan đã thực hiện theo quy định và ý kiến của cơ quan quản lý chuyên ngành (Cục Quản lý dược – Bộ Y tế) về thời hạn còn lại của thuốc khi đến cảng Việt Nam.
Như vậy, cho đến thời điểm này, cả Bộ Y tế và Bộ Tài chính đều khẳng định việc cấp phép và thông quan cho 20.000 viên thuốc Tasigna (nilotinib) 200mg đặc trị ung thư của hai đơn vị trên đều được tiến hành đúng quy trình.
Tuy nhiên, câu hỏi nguyên nhân vì sao mà 20.000 viên thuốc đặc trị ung thư đắt tiền trên lại bị lưu kho đến hết hạn, lãng phí hơn chục tỷ đồng vẫn là một uẩn khúc cần được các cơ quan chức năng làm sáng tỏ trong thời gian tới.
